ニュース&イベント NEWS & EVENTS
doxepin幾何異性体のヒスタミンH1受容体結合における熱力学的特性を解明
~エンタルピー-エントロピー補償の内訳に基づいた評価手法を確立~
研究の要旨とポイント
- ヒスタミンH1受容体(H1R)とdoxepin幾何異性体(E-doxepinおよびZ-doxepin)の結合を等温滴定型カロリーメーター(ITC)で直接測定し、熱力学パラメータを定量化することに成功しました。
- 分子動力学(MD)シミュレーションにより、親和性の高いZ-doxepinにおいて見られたエンタルピー-エントロピー補償が、受容体結合時にリガンドの立体構造が制限されることに起因することを明らかにしました。
- 本研究成果は、Gタンパク質共役型受容体(GPCR)標的薬の開発において新たな方向性を示すものであり、特に立体異性体を考慮した薬剤設計や、受容体変異に応じた個別化医療の実現に役立つことが期待されます。
研究の概要
東京理科大学 先進工学部 生命システム工学科の白石 充典教授、同学部 電子システム工学科の安藤 格士准教授、同大学大学院 先進工学研究科 生命システム工学専攻の金子 大斗氏(2025年度 博士課程1年)および東京大学の研究グループは、等温滴定型カロリーメーター(ITC)と分子動力学(MD)シミュレーションを組み合わせ、ヒスタミンH1受容体(H1R)とdoxepinの幾何異性体(E-doxepinおよびZ-doxepin、*1)との結合を熱力学的に解析することに成功しました。
Gタンパク質共役型受容体(GPCR)はヒトにおいて最も大きなタンパク質ファミリーであり、最大の創薬標的です。近年の創薬において、単に化合物と標的タンパク質の親和性(結合エネルギー)だけでなく、その内訳であるエンタルピーとエントロピーに基づいた化合物設計の重要性が提唱されています。しかし、GPCRのような膜タンパク質では、受容体とリガンドの結合における熱力学パラメータを直接測定した例は限られていました。
本研究では、出芽酵母発現系を用いた受容体調製により、H1Rとdoxepin幾何異性体の結合をITCで直接測定しました。また、MDシミュレーションから、親和性の高いZ-doxepinの結合において観察されたエンタルピー-エントロピー補償(*2)が、結合時のリガンドの立体構造制限によるものであることを明らかにしました。
本研究により、GPCRとリガンドの結合におけるエンタルピーとエントロピーの相補的関係の仕組みが解明されました。この成果は、優れた熱力学的特性と薬理機能を持つリガンドを設計する上で、立体構造の制限性と柔軟性を適切に制御することが極めて重要であることを示しています。
本研究成果は、2026年1月26日に国際学術誌「ACS Medicinal Chemistry Letters」にオンライン掲載されました。
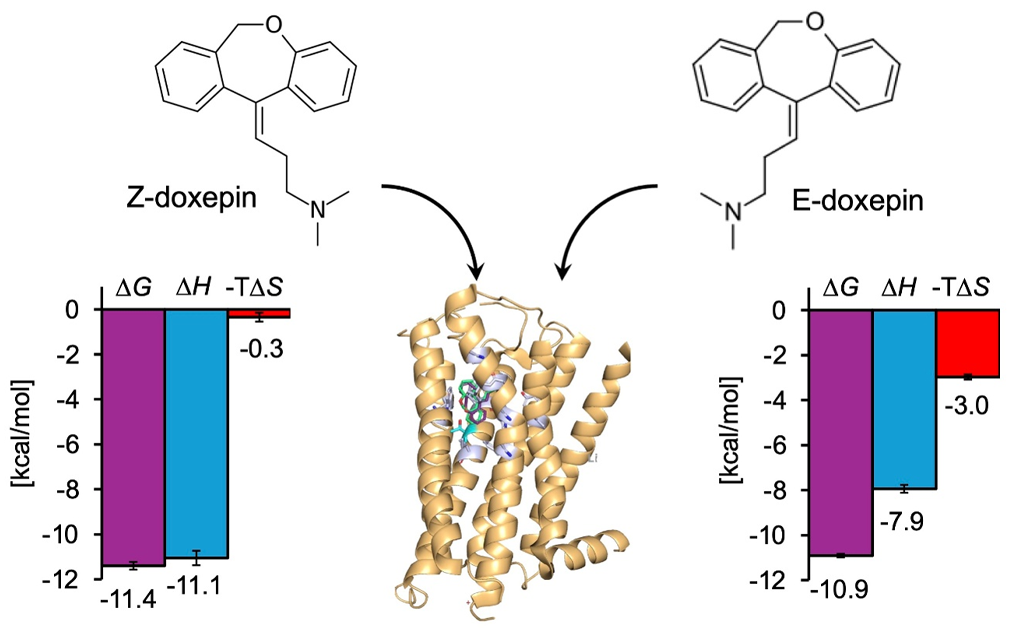
受容体結合時のZ-doxepinおよびE-doxepinの熱力学パラメータを定量化することに成功した。
研究の背景
Gタンパク質共役受容体(GPCR)は、ホルモン、神経伝達物質、薬物を認識して多様なシグナル伝達を制御する膜タンパク質ファミリーであり、現在市販されている医薬品の30%以上がGPCRを標的としています。
ヒスタミンH1受容体(H1R)はGPCRのサブタイプで、アレルギー・炎症反応、血管透過性、気道収縮、中枢神経系における覚醒・認知機能の調節に関与しています。H1Rは抗ヒスタミン薬の主要標的ですが、第一世代抗ヒスタミン薬は鎮静などの副作用があり、第二世代抗ヒスタミン薬はそれらの副作用が改善されたものの治療効果が限定的な場合があるため、新たな視点からのリガンド探索が求められています。
三環系抗うつ薬doxepinは強力な抗ヒスタミン薬であり、2種類の幾何異性体(E-doxepinとZ-doxepin)として存在しています。本研究グループはこれまでの研究により、Z-doxepinがE-doxepinよりもH1Rに対して約5倍強く結合すること、Thr1123.37が異性体選択の鍵となる残基であることを見出していました(※1)。そこで本研究では、これらのエントロピー-エンタルピー補償の内訳を調べ、異性体の相互作用の詳細を明らかにすることを目指しました。
※1: 東京理科大学プレスリリース(2024年7月1日付)
抗ヒスタミン薬Doxepinの異性体による結合特性のちがいを解明 ~次世代抗ヒスタミン剤の設計へ向けた新たな知見~
研究結果の詳細
等温滴定型カロリーメーター(ITC)を用いて、野生型H1Rおよび変異型H1R(T1123.37V)とdoxepinとの相互作用について熱力学的解析を行いました。その結果、野生型と変異型における結合親和性に有意差は認められませんでしたが、エンタルピーおよびエントロピーの寄与は大きく異なることが明らかとなりました。野生型H1Rとの相互作用はエンタルピー駆動型であり、大きなエンタルピー利得と比較的小さなエントロピー寄与を示しました。このエンタルピー利得は、主にファンデルワールス力などの非極性相互作用の形成に起因していると考えられます。一方、変異型H1Rとの相互作用では、エンタルピーの寄与が小さく、エントロピーの寄与が大きくなることがわかりました。これらの結果は、Thr1123.37がH1Rのdoxepin認識において、エンタルピー的な安定化に重要な役割を果たしていることを示唆しています。
野生型H1Rに対する2つの異性体の熱力学パラメータを比較すると、Z-doxepinはE-doxepinよりもエンタルピー利得が3.2 kcal/mol、エントロピー損失が2.6 kcal/mol大きいことがわかりました。対照的に、変異型H1Rでは、両異性体のエンタルピーとエントロピーに大きな違いは見られませんでした。以上のことから、Thr1123.37のヒドロキシ基がリガンド結合時のエンタルピー利得とエントロピー損失のバランスに寄与しており、特にZ-doxepinとの相互作用において顕著な影響を及ぼすことで、異性体選択性が生じていることが示唆されました。
分子動力学(MD)シミュレーションを用いて、受容体結合前後におけるdoxepinの立体構造についてクラスター分析を行いました。受容体結合前および変異体H1R結合後は、両異性体とも類似した広いクラスター分布を示しました。しかし、野生型H1Rに結合した場合、E-doxepinは広いクラスター分布を維持したのに対し、Z-doxepinの分布は複数のクラスターに顕著に偏ることがわかりました。これらの結果から、野生型H1Rにおいては、Thr1123.37のヒドロキシ基によってZ-doxepinが受容体の結合部位にフィットし、特定の立体構造が安定化されることで、立体構造エントロピーの減少と引き換えに、より大きなエンタルピーの利得が得られることが示唆されました。この解釈はITCによる解析結果と一致しており、Z-doxepinの野生型H1Rへの結合は、E-doxepinと比較してより大きなエンタルピー利得とより大きなエントロピー損失を伴うことが、実験と理論計算の両方から明らかになりました。
本研究を主導した白石教授は、「本研究で用いた「エンタルピー-エントロピー補償の内訳に基づいた化合物の評価」は、今後のGPCR創薬において新たな指針となることが期待されます。特に、異性体や立体化学を活かした薬剤設計や変異受容体に対する精密医薬の開発に貢献できると考えています。さらに、相互作用の熱力学的解析とMDシミュレーションを組み合わせた解析手法は、他のGPCRやタンパク質にも展開可能であり、合理的なリード最適化やAI創薬へのデータ基盤としての応用も期待されます」と、コメントしています。
※ 本研究は、日本学術振興会(JSPS)の科研費(JP25709080, JP19K06514)、国立研究開発法人 日本医療研究開発機構(AMED)の創薬等ライフサイエンス研究支援基盤事業(創薬等支援技術基盤プラットフォーム(BINDS); JP24ama121033)、国立研究開発法人 科学技術振興機構(JST)の次世代研究者挑戦的研究プログラム(SPRING; JPMJSP2151)の助成を受けて実施されました。
用語
*1 幾何異性体
炭素–炭素二重結合(C=C)などの回転が制限される構造に起因して生じる立体異性体。置換基の優先順位をカーン・インゴールド・プレローグ順位則(CIP順位則)に基づいて評価し、高順位の置換基が二重結合を挟んで反対側に位置する場合をE体、同じ側に位置する場合をZ体と定義する。
*2 エンタルピー-エントロピー補償
エンタルピー変化(ΔH)とエントロピー変化(ΔS)が相反的に変化し、その結果、自由エネルギー変化(ΔG = ΔH-TΔS)がほぼ一定に保たれる現象。受容体とリガンドの結合過程において、例えば、強い水素結合や静電相互作用の形成はエンタルピー的に有利である一方、分子や溶媒の自由度が低下するためエントロピー的には不利となることが多い。一方、疎水性相互作用は水分子の秩序化を解放するためエントロピー的に有利となるが、エンタルピー的な寄与は小さい傾向にある。
論文情報
雑誌名
ACS Medicinal Chemistry Letters
論文タイトル
Enthalpy–entropy trade-off underlies geometric isomer selectivity in histamine H1receptor–doxepin interaction
著者
Hiroto Kaneko, Satoru Nagatoishi, Kouhei Tsumoto, Tadashi Ando, Mitsunori Shiroishi
