ニュース&イベント NEWS & EVENTS
認知症の簡便な診断につながる新技術を開発
~血液中の神経損傷マーカーをとらえる核酸分子を発見、次世代診断法への応用に期待~
東京理科大学
国立大学法人東京農工大学
研究の要旨とポイント
- 認知症などの神経変性疾患では、血液中に神経損傷マーカーであるNfLが増加することが知られていますが、これまで正確に測定する方法は限られていました。
- 本研究では、NfLに特異的に結合する核酸分子を発見しました。これを用いることで血液中のNfLを正確に検出できました。
- 将来的に、認知症を含む神経変性疾患の診断や経過観察など幅広い用途に活用できると期待されます。
研究の概要
東京理科大学 理学部第一部 化学科の塚越 かおり准教授、東京農工大学 大学院工学府生命工学専攻の松元 美優氏(博士前期課程2年)、同大学 大学院工学研究院生命機能科学部門の池袋 一典卓越教授の研究グループは、血液中に存在する神経損傷マーカーであるNeurofilament light chain(ニューロフィラメント軽鎖、NfL)を、微量でも高精度に検出可能な新規DNAアプタマー(*1)を発見しました。今後アルツハイマー病の進行度診断など多様な応用が見込まれます。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の戦略的国際共同研究プログラム(SICORP(JP22jm0210099))として日英共同研究課題として実施された成果です。
NfLは、認知症をはじめとするさまざまな神経変性疾患で、血中で増加することが報告されています。そのため近年、血液検査で病気の進行度評価に活用可能なバイオマーカー(*2)として注目されています。一方で、血液中のNfLは微量で正確に検出するためのリガンド(*3)も限られているため、NfLを高精度に測定する装置や技術の開発が課題となっています。
そこで本研究グループは、NfLを正確に捉えるためのリガンドの開発を目指し、合成DNAでできたリガンドであるDNAアプタマーに着目しました。DNAアプタマーは完全化学合成できることから、さまざまな官能基を修飾可能という研究開発上の大きな利点があります。そこで、多様な塩基配列をもつDNAライブラリからスクリーニングを行い、血液中のNfLに選択的に結合するDNAアプタマーを見つけ出しました。このアプタマーは市販の抗体に匹敵する結合親和性を有していることも確認しました。
本アプタマーの開発により、利便性の高いNfL測定装置の実現可能性が広がり、血液検査による神経変性疾患の状態評価法の開発が進むことが期待されます。将来的には、認知症を含む疾患の診断や経過観察を支える技術へと発展し、早期かつ適切な診断を通じて治療薬等の投与判断に資することで、高齢化社会における認知症医療の推進に貢献する可能性があります。
本研究成果は、2026年1月18日に国際学術誌「Biochemical and Biophysical Research Communications」にオンライン掲載されました。
研究の背景
認知症をはじめとする神経変性疾患では、脳や神経の損傷が進むにつれて、日常生活への影響が大きくなります。適切な治療やケアの方針を考えるためには、早い段階から疾患の状態を正しく把握し、病気の進行具合を客観的に知る手段が必要です。近年、その有力な候補として、採血で測定可能なバイオマーカーが注目されています。
NfLは神経に存在するタンパク質で、神経が損傷すると血液中に放出されます。これまでの研究から、NfLは認知症だけでなくさまざまな神経変性疾患で血中濃度が増加することが分かっていました。そのためNfLは、血液検査で病気の進行度を把握する手がかりになるとして期待されています。
しかしながら、血液中のNfLは極めて微量であるため、正確に測定するにはNfLを高い親和性で捉えるリガンドが必要です。これまでのリガンド開発は、標的となるタンパク質上の異なるエピトープ(抗原結合部位)を認識する2種類の抗体ペア(モノクローナル抗体ペア)の探索を中心に進められてきましたが、血液中でNfLを安定して捉えられるモノクローナル抗体ペアは限られています。さらに、そうしたモノクローナル抗体は培養細胞を用いて生成するという性質上、ロット間変動のおそれや化学修飾できる官能基の種類に制限があり、より安定的に製造できるリガンドの開発が求められています。
そこで本研究では、利便性の高いNfL測定装置の開発に向け、新たなリガンド候補としてDNAアプタマーに注目しました。DNAアプタマーはSELEX(Systematic Evolution of Ligands by Exponential Enrichment、試験管内進化法*4)と呼ばれる技術によって開発される一本鎖オリゴヌクレオチドです。DNAアプタマーは標的となるタンパク質との結合において親和性や特異性を示すことが報告されています。さらに、完全化学合成が容易であるため、製造時のロット間変動を最小限に抑えることができ、製造コストが低く直接的な化学修飾も容易可能です。これらの特性から、DNAアプタマーは、電気化学的測定法、光学的測定法、またはマイクロ流体デバイスなどと組み合わせバイオセンサーが開発でき、利便性の高いプラットフォームでの検出が可能になると期待されます。
研究結果の詳細
本研究では、血液中のNfLを正確に捉えるDNAアプタマーを得ることを目的に、SELEXという方法を用いて候補分子を選抜しました(図1)。選抜で得られたDNA配列を解析したところ、86種類の異なる配列が見つかり、その多くはグアニン(*5)を多く含んでいました。グアニンを多く含むDNAは、条件によってはDNA同士が集まって塊になってしまうことが多く、測定が不安定になる要因となります。そこで、Native PAGE(*6)という電気泳動方法を使って塊ができていないかを確認し、安定して扱える候補アプタマーを選抜し、以下の評価試験に進めました。
次に、アプタマーブロッティング(*7)を用いて、候補アプタマーがNfLのどの領域に結合するかを解析しました。その結果、この候補は全長NfLに結合し、特にNfLの281〜338番目のアミノ酸を含む断片に強く結合しました。一方、381〜543番目のみを含む断片にはほとんど結合しませんでした。したがって候補アプタマーは、この領域を主に認識していることが分かりました。認知症では、281〜338番目の領域を含むNfLが血液中で増加しているとされています。そのため、アプタマーは血液中のNfLを捕捉できるリガンドであることがわかりました。
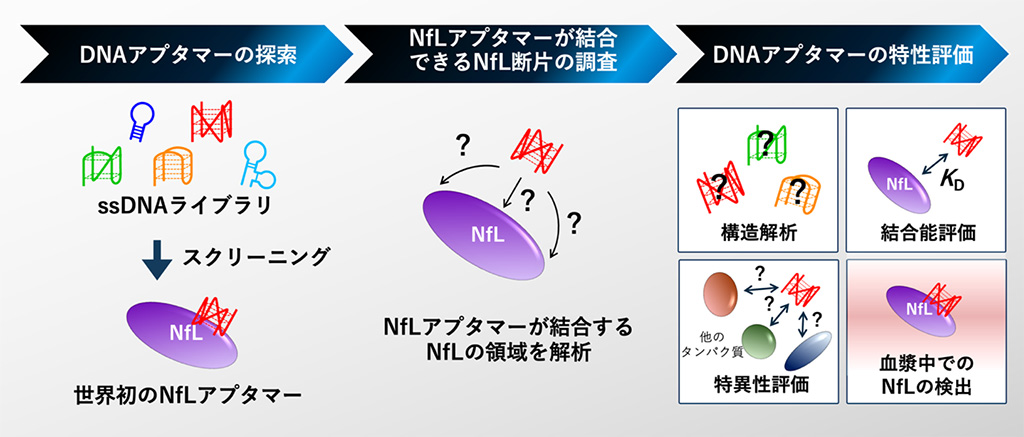
候補アプタマーの中から、MN711とMN734という2種類について、性質を詳しく調べました。円二色性スペクトル測定(*8)により、分子の立体構造の特徴を解析したところ、どちらもグアニン四重鎖構造(*9)と呼ばれる特徴的な立体構造を取っていることが分かりました。さらにNfLとの結合を評価したところ、どちらもごく低濃度のNfLでも結合が検出でき、結合力は現在広く用いられている抗NfL抗体と同程度でした。
最後に、ヒト血漿にNfLを添加した試料でMN711の性能を評価しました。その結果、NfL濃度の上昇に応じて反応強度が高まったことから、血液成分を含む条件下でも十分に機能することが確認されました。
本アプタマーの開発により、利便性の高いNfL測定装置の実現可能性が広がり、血液検査で神経変性疾患の状態を調べる新たな方法の開発が進むことが期待されます。将来的には、認知症を含む疾患の診断や経過観察を支える技術へと発展し、早期かつ適切な診断を通じて治療薬等の投与判断に資することで、高齢化社会における認知症医療の推進に貢献する可能性があります。
※ 本研究は、AMED-SICORP(JP22jm0210099)、公益財団法人吉田育英会大学院生給与奨学金<マスター21>の助成を受けて実施したものです。
用語
*1 DNAアプタマー
特定のタンパク質などに強く結合するように設計・選抜された短いDNA分子。
*2 バイオマーカー
病気の有無や進行度、治療効果などを客観的に示す指標となる体内の物質。
*3 リガンド
受容体やタンパク質などの標的分子に結合する分子(抗体、アプタマー、低分子化合物など)。
*4 SELEX(Systematic Evolution of Ligands by Exponential Enrichment)
多数のDNA候補から、標的に結合するものを選別する手法。
*5 グアニン
DNAを構成する4種類の塩基の1つ(G)。配列中に多く含まれていると特定の立体構造を作りやすいなどの特徴がある。
*6 Native PAGE
タンパク質や核酸を変性させず、元の立体構造や集合状態を保ったまま電気泳動で分離する方法。
*7 アプタマーブロッティング
膜上に固定した標的に対してアプタマーを反応させ、結合の有無や結合部位の違いを検出する手法。
*8 円二色性スペクトル測定
円偏光(二種類の偏光)の吸収差を測り、分子(DNAやタンパク質)の立体構造の特徴を調べる方法。
*9 グアニン四重鎖構造
グアニンが多い配列が作る四重らせん状の立体構造。
論文情報
雑誌名
Biochemical and Biophysical Research Communications
論文タイトル
Competitive-SELEX discovery of DNA aptamers selective for neurofilament light chain in human plasma
著者
Miyu Matsumoto, Kazunori Ikebukuro, Kaori Tsukakoshi
DOI
発表者
- 松元美優
- 東京農工大学 大学院工学府 生命工学専攻 博士前期課程2年<共同筆頭著者>
- 池袋⼀典
- 東京農工大学 大学院工学研究院 生命機能科学部⾨ 卓越教授<共同責任著者>
- 塚越かおり
- 東京理科大学 理学部第一部 化学科 准教授<共同筆頭著者、共同責任著者>
